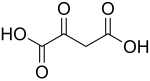
Щавелевоуксусная кислота
Щавелевоуксусная кислота (оксалоацетат, оксобутандиовая кислота, Oxaloacetic acid, oxaloacetate) — дикарбоновая кислота (четырёхуглеродная двухосновная кетокислота). Играет важную биологическую роль: является промежуточным звеном цикла лимонной кислоты, где вступает в реакцию с ацетил-КоА с образованием цитрата, катализируемого цитратсинтазой. Участвует в глюконеогенезе, цикле мочевины, цикле глиоксилата, синтезе аминокислот и синтезе жирных кислот. Также является мощным ингибитором комплекса II. Обладает химической формулой HO2C-C(O)-CH2-CO2H[1].
Физические свойства[править | править код]
Температура плавления 161°C. Температура кипения: 341,9°C.
Молекулярный вес (молярная масса) 132,07 г/мол.
Плотность 0,18 г/см3.
Цис-изомер (см. ниже) представляет собой бесцветные кристаллы с температурой плавления 152°, растворимые в воде, спирте, ацетоне, этилацетате, нерастворимые в бензоле и хлороформе. Транс-изомер — бесцветные кристаллы с с температурой плавления 184°, при нагревании до 50° переходит в транс-изомер.
Растворяется в эфире, воде и спирте.
Химические свойства[править | править код]
Соли и эфиры щавелевоуксусной кислоты называются оксалоацетатами.
В кислых растворах декарбоксилируется.
При взаимодействии с металлами образует их оксалоацетаты, например оксалоацетат натрия:
HO2C-C(O)-CH2-CO2H + 2Na → NaО-СО-СО-CH2-СО-ONa + H2↑
Взаимодействие с основными оксидами также даёт оксалоацетат:
HO2C-C(O)-CH2-CO2H + Na2O → NaО-СО-СО-CH2-СО-ONa + H2O
При реакции с аммиаком при нагревании даёт 2-оксобутандиамид:
HO2C-C(O)-CH2-CO2H + 2NH3 → H2N-СО-СО-CH2-СО-NH2 + 2H2O
При гидрировании превращается в яблочную кислоту:
HO2C-C(O)-CH2-CO2H + H2 → НООС−СН2−СН(ОН)−СООН
Подвергается последовательному депротонированию, чтобы дать дианион:
- HO2CC(O)CH2CO2H ⇌ −O2CC(O)CH2CO2H + H+, pKa = 2.22
- −O2CC(O)CH2CO2H ⇌ −O2CC(O)CH2CO2− + H+, pKa = 3.89
При высоком рН енолизируемый протон ионизируется:
- −O2CC(O)CH2CO2− ⇌ −O2CC(O−)CHCO2− + H+, pKa = 13.03
Енольные формы щавелевой уксусной кислоты особенно стабильны, настолько, что два таутомера имеют разные температуры плавления (152 °C для цис-изоформы и 184 °C для транс-изоформы). Эта реакция катализируется ферментом оксалоацетат таутомеразой. транс-Енол-оксалоацетат также появляется, когда тартрат является субстратом для фумаразы
Получение[править | править код]
Получена Неффом из этилового эфира оксифумаровой кислоты СО2НС(ОН)СНСО2Н, которая таутомерна щавелевоуксусной кислоте и представляет её энольную форму. Для получения данной кислоты эфир омыляется при кипячении алкогольным раствором едкого кали, образовавшаяся калийная соль разлагается слабой серной кислотой, свободная кислота очищается кристаллизацией из эфира.
Получают путём окисления L-яблочной кислоты.
В природе образуется несколькими способами. Основным путем является окисление L-малата, катализируемое малатдегидрогеназой, в цикле лимонной кислоты. Малат также окисляется сукцинатдегидрогеназой в медленной реакции, причем исходным продуктом является енол-оксалоацетат.
Также возникает в результате конденсации пирувата с углекислотой, обусловленной гидролизом АТФ:
- CH3C(O)CO2− + HCO3− + ATФ → −O2CCH2C(O)CO2− + АДФ + Pi
Происходящий в мезофилле растений, этот процесс протекает через фосфоенолпируват, катализируемый фосфоенолпируваткарбоксилазой. Оксалоацетат также может образовываться в результате транс - или деаминирования аспарагиновой кислоты.
Эфиры[править | править код]
Диэтилоксалоацетат (диэтиловый эфир щавелевоуксусной кислоты, щавелевоуксусный эфир, C2H5OC(O)CH2COCOOC2H5) может производится с помощью конденсации этилацетата с диэтилоксалатом в присутствии металлического натрия или этилата натрия C2H5ONa. Используется в органическом синтезе.
Аналитическая химия[править | править код]
Количественно щавелевоуксусную кислоту определяют колориметрически в виде 2,4-динитрофенилгидразона или манометрически по объёму диоксида углерода, выделившегося при декарбоксилировании щавелевоуксусной кислоты.
Биохимический аспект[править | править код]
Является исходным веществом цикла трикарбоновых кислот (цикла Кребса).
Точнее, является промежуточным соединением в цикле Кребса и глюконеогенезе. Образуется при окислении малата, катализируемого малатдегидрогеназой.
Взаимодействует с ацетил-КоА, образуя цитрат, при участии фермента цитратсинтазы.
Также образуется в мезофилле растений, путём конденсации углекислого газа с фосфоенолпируватом, катализируемой фосфоенолпируваткарбоксилазой.
Образуется из пирувата в анаплеротической реакции.
Из щавелевоуксусной кислоты и ацетил кофермента А по типу альдольной конденсации происходит биосинтез лимонной кислоты.
Недостаток щавелевоуксусной кислоты нарушает нормальное течение цикла Кребса и вызывает расстройства обмена веществ и энергии.
Данная кислота служит веществом, связывающим между собой углеводный обмен и обмен аминокислот. Также она участвует в процессах трансаминирования.
В природе данная кислота существует в виде двух таутомерных форм — енольной и кетонной (HOOC—CO—CH2—COOH, кетоянтарная кислота) и в виде цис-транс-изомеров. Транс-изомер данной кислота называют оксифумаровой кислотой), транс-изомер — оксималеиновой кислотой.
В организме животных и человека щавелевоуксусная кислота синтезируется из пировиноградной кислоты и CO2 либо продуцируется из аспарагиновой кислоты в ходе трансаминирования.
При недостатке щавелевоуксусной кислоты в печени накапливаются ацетильные группы, не способные к окислению, которые начинают быстро превращаться в кетоновые тела. Их избыточное образование ведёт к развитию метаболического ацидоза и прочим патологическим состояниям. Кетоз, как правило сопутствующий нарушению баланса между окислением жиров и катаболизмом углеводов, появляется во всех случаях относительной нехватки щавелевоуксусной кислоты по сравнению с КоА, когда ацетил-КоА не может полностью вступить в реакцию конденсации с оксалоацетатом (то есть в первую реакцию цикла Кребса). Такой недостаток щавелевоуксусной кислоты может возникать в условиях необходимости метаболизирования в печени больших количеств этанола, при голодании либо сахарном диабете.
- ↑ Большая медицинская энциклопедия / гл. ред. Б. В. Петровский. — 3-е изд. — М.: Советская энциклопедия, 1974—1989. — Т. 1—30.